Vaccino COVID-19 mRNA BNT162b2 Istruzioni per l’uso.
Germania, iniettate 5 dosi vaccino per errore a 8 sanitari
A seguito “dell’incidente” avvenuto in Germania, dove per errore, il 28 dicembre a otto dipendenti, di una casa di cura per anziani, sono state iniettate anziché una, ben 5 dosi di vaccino antiCovid a testa. Cosicché quattro di loro, sono finiti in ospedale precauzionalmente in stretta osservazione, avendo gli stessi, manifestato leggeri sintomi influenzali subito dopo.
Riteniamo pertanto utile far conoscere a tutti, quali sono le articolate regole, che gli operatori sanitari debbono seguire, sia nel maneggiare il vaccino, sia nella sua somministrazione ed anche per la conservazione.
mRNA BNT162b2: un concentrato particolare per soluzione iniettabile
Essendo in pieno periodo di somministrazione del vaccino COVID-19 mRNA BNT162b2, prodotto da BioNTech, Fosun Pharma, Pfizer. Riteniamo che possa essere utile condividere con i Cittadini alcune informazioni, elaborate sulla base della letteratura e del riassunto delle caratteristiche del prodotto, ormai autorizzato da più Autorità e anche dall’OSM.
La presente istruzione operativa riguarda, pertanto, le procedure previste per il vaccino COVID-19 mRNA BNT162b2, somministrabile a pazienti adulti e adolescenti, di età maggiore ai 16 anni.
Che cos’è e a che cosa serve?
Il vaccino COVID-19 mRNA BNT162b2 (Comirnaty) è un vaccino destinato a prevenire la malattia da coronavirus 2019 (COVID-19) nei soggetti di età pari o superiore a 16 anni. Contiene una molecola denominata RNA messaggero (mRNA) con le istruzioni per produrre una proteina presente su SARSCoV-2, il virus responsabile di COVID-19.
Il vaccino non contiene il virus e non può provocare la malattia
COMPOSIZIONE QUALITATIVA E QUANTITATIVA
Fiala multi-dose da diluire prima dell’uso.
1 fiala (0,45 mL) contiene 5 dosi di 30 microgrammi di mRNA BNT162b2 ciascuna (incorporato in nanoparticelle lipidiche).
In ciascuna fiala sono presenti anche, l’RNA messaggero, che è racchiuso in liposomi, formati da ALC-0315 ((4-idrossibutil)azanediil)bis(esano6,1-diil)bis(2-esildecanoato) e ALC-0159 (2-[(polietilenglicole)-2000]-N,N-ditetradecilacetammide). ALC-0315 e ALC-0159 sono lipidi sintetici che contribuiscono a formare le vescicole che veicolano il vaccino.
Il vaccino contiene inoltre altri eccipienti:
• 1,2-Distearoyl-sn-glycero-3-phosphocholine
• colesterolo
• Potassio cloruro
• Potassio diidrogeno fosfato
• Sodio cloruro
• Fosfato disodico diidrato
• saccarosio
• acqua per preparazioni iniettabili
Non è presente un sistema conservante. Il contenuto totale di potassio è inferiore a 1 mmol (39 mg) per dose.
POSOLOGIA
Solo per Individui di età pari o superiore a 16 anni
Il vaccino COVID-19 mRNA BNT162b2 viene somministrato per via intramuscolare. Il trattamento prevede la somministrazione di due dosi da 0,3 mL ciascuna, somministrate a distanza di 21 giorni.
Non ci sono dati disponibili su l’intercambiabilità del vaccino COVID-19 mRNA BNT162b2 con altri vaccini COVID-19 per completare la serie di vaccinazioni. Individui che hanno ricevuto una dose del vaccino COVID-19 mRNA BNT162b2 devono ricevere una seconda dose di COVID-19 mRNA
BNT162b2 per completare la serie di vaccinazioni.
Gli individui potrebbero non essere protetti fino ad almeno 7 giorni dopo la loro seconda dose di vaccino.
La durata della protezione non è ancora definita con certezza perché il periodo di osservazione è stato necessariamente di pochi mesi, ma le conoscenze sugli altri tipi di coronavirus indicano che la protezione dovrebbe essere di almeno 9-12 mesi.
MODALITÁ DI ALLESTIMENTO E SOMMINISTRAZIONE
Somministrare il vaccino COVID-19 mRNA BNT162b2 per via intramuscolare in un muscolo della parte superiore del braccio (muscolo deltoide) dopo la diluizione.
Non iniettare il vaccino per via intravascolare, sottocutanea o intradermica.
Dispositivi necessari all’operazione di allestimento e somministrazione:
– Siringa da 3 mL + ago 21G per il prelievo di cloruro di sodio 9 mg/mL (0,9%) e la successiva diluizione del vaccino;
– Siringa da 1 mL per il prelievo e somministrazione della dose di 0,3 mL;
– Aghi per la somministrazione da 23G o 25 G.
Laddove la somministrazione sia immediatamente successiva all’allestimento, è indispensabile adottare le necessarie precauzioni per evitare di contaminare la preparazione:
- disinfettare il ripiano con alcool etilico 70%,
- delimitare il campo per l’allestimento con adeguato telo sterile,
- utilizzare guanti sterili
- utilizzare i necessari Dispositivi di Protezione Individuale.
Indicazioni dettagliate da seguire prima dell’uso
Le fiale congelate a -75°C devono essere trasferite a 2-8 °C  per farle scongelare lentamente; una confezione da 195 fiale può richiedere 3 ore per scongelare.
per farle scongelare lentamente; una confezione da 195 fiale può richiedere 3 ore per scongelare.
In alternativa, le fiale congelate possono anche essere scongelate per 30 minuti a massimo 25 °C per un utilizzo immediato.
Una volta scongelato, il vaccino non diluito può essere conservato per un massimo di 5 giorni a una temperatura compresa tra 2 °C e 8 °C ovvero fino a 2 ore a temperature fino a 25 °C.
Attendere che la fiala congelata ovvero conservata a 2-8 °C raggiunga la temperatura ambiente prima di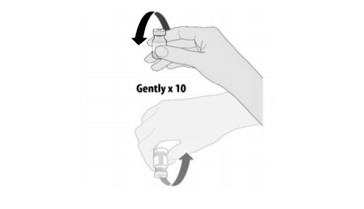
procedere con le operazioni di diluizione.
Capovolgere delicatamente 10 volte prima della diluizione. Non agitare.
Prima della diluizione il vaccino dovrebbe presentarsi come una soluzione biancastra senza particolato visibile. Scartare il vaccino se sono presenti particelle o alterazioni di colore.
Attenzione
Il vaccino scongelato deve essere diluito nella sua fiala originale.
Disinfettare con una garza imbevuta di alcool etilico al 70% l’elastomero della fiala e diluire con 1,8 mL di soluzione iniettabile di cloruro di sodio 9 mg/mL (0,9%), utilizzando una siringa da 3ml un ago calibro 21 Gauge o superiore e tecnica asettica.
Avvertenza: La soluzione iniettabile di cloruro di sodio 9 mg/mL (0,9%) senza conservanti è il solo diluente che deve essere usato. Questo diluente non è fornito nella confezione del vaccino.
La procedura di diluzione deve essere completata entro 2 ore dal momento in cui la fiala è stata scongelata o prelevata dal frigorifero a 2-8 °C.
Prima di rimuovere l’ago, equalizzare la pressione della fiala, prelevando 1,8 mL di aria nella
siringa diluente vuota.
Capovolgere delicatamente 10 volte la fiala. Non agitare.
Il vaccino diluito dovrebbe presentarsi come una soluzione biancastra senza particolato visibile.
Scartare il vaccino diluito se sono presenti particolato o cambiamenti di colore.
Segnare sulla fiala la data e ora di limite utilizzo.
Utilizzare immediatamente o comunque entro 6 ore dalla diluizione, conservando la fiala ad una temperatura compresa tra 2 e 25 °C.
Dopo la diluizione, la fiala contiene 5 dosi da 0,3 mL.
Disinfettare la superficie della fiala con una garza imbevuta di alcool etilico 70% e poi prelevare 0,45 mL, utilizzando una siringa da 1 mL con un ago calibro 23 o 25 Gauge. Siringa ed ago devo essere sterili.
Eliminare tutte le bolle ed espellere il medicinale in eccesso premendo lentamente lo stantuffo in modo che la si allinei alla linea che segna 0,3 mL sulla siringa.
Rimuovere l’ago dalla fiala. Preparare tutte e 5 le siringhe in continuità
Preferibilmente cambiare successivamente l’ago con uno idoneo alla somministrazione intramuscolare.
Al termine delle somministrazioni, la fiala con il vaccino residuo deve essere smaltita seguendo i protocolli standard.
La somministrazione come deve essere effettuata
La vaccinazione sarà effettuata da medici e infermieri dei servizi vaccinali pubblici, persone che da tempo praticano vaccinazioni e sono esperte nelle tecniche di vaccinazione. Inoltre, in considerazione della particolarità di questo vaccino, gli operatori sanitari hanno ricevuto ulteriori informazioni tecniche specifiche sulla preparazione e somministrazione del vaccino COVID-19 mRNA BNT162b2 (Comirnaty).
Il vaccino COVID-19 mRNA BNT162b2 (Comirnaty) viene somministrato in due iniezioni, solitamente nel muscolo della parte superiore del braccio, a distanza di almeno 21 giorni l’una dall’altra.
Un documento di identità valido e la tessera sanitaria. Può essere utile avere con sé anche l’eventuale documentazione sanitaria che possa aiutare il medico vaccinatore a valutare lo stato fisico.
PRECAUZIONI PARTICOLARI PER LA CONSERVAZIONE
Conservare:
- la soluzione di vaccino non diluito in congelatore a una temperatura compresa tra -80 ° C e -60 ° C per 6 mesi. Comunque i dati di stabilità indicano che una volta scongelato il vaccino può essere conservato per un massimo di 5 giorni tra 2-8 °C.
- nel contenitore termico a una temperatura compresa tra -90 ºC e -60 ºC per 15 giorni, cambiando ogni 5 giorni il ghiaccio secco contenuto.
- Conservare nella confezione originale per proteggere il medicinale dalla luce.
- Dopo lo scongelamento, il vaccino a una temperatura tra 2 e 8 °C per 5 giorni ovvero deve essere diluito e utilizzato immediatamente. Comunque, i dati di stabilità indicano che una volta portato a temperatura non superiore a 25 °C il vaccino non diluito può essere conservato per un massimo di 2 ore.
- Dopo la diluizione il vaccino tra 2 e 25 °C, usare immediatamente oppure entro le 6 ore.
- Una volta diluito, apporre sulla fiala la data, l’ora di limite utilizzo (6 ore dalla diluizione). Una volta scongelato, il vaccino non può essere ricongelato.
Al termine della somministrazione delle 5 dosi di vaccino, smaltire la fiala e l’eventuale residuo di vaccino non utilizzato.
TRACCIABILITÁ
Allo scopo di assicurare la tracciabilità del vaccino, si deve registrare per ogni somministrazione effettuata:
nome del paziente, denominazione del medicinale, numero di lotto e data di scadenza del farmaco somministrato.
SORVEGLIANZA VACCINO COVID-19
La segnalazione di una qualsiasi reazione alla somministrazione del vaccino può essere fatta al proprio medico di famiglia o alla ASL di appartenenza, così come per tutte le altre reazioni avverse a qualunque farmaco, secondo il sistema nazionale di farmacovigilanza attivo da tempo in tutto il Paese.
Inoltre, chiunque può segnalare in prima persona una reazione avversa da vaccino utilizzando i moduli pubblicati sul sito AIFA:
https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse
Inoltre tali segnalazioni, devono essere tempestivamente effettuate, entro 36 ore dal medico o l’operatore sanitario, che ne viene a conoscenza, direttamente online, sul sito VigiFarmaco (https://www.vigifarmaco.it/), oppure compilando, la scheda di segnalazione cartacea e inviandola al Responsabile di Farmacovigilanza, della propria struttura di appartenenza, via e-mail o fax.
Movimento CittadiniNelCuore
Fonti: http://Vaccino COVID-19 mRNA BNT162b2 Istruzioni per l’uso. http://www.quotidianosanita.it/allegati/allegato8388668.pdf




